제 6 강 반응속도와 화학평형
■화학반응의 속도
.화학반응
화학(반응)물질의 변화에 수반되는 일련의 과정
화학적 변화를 일으키며, 반응물지과 성질이 다른 물질을 생성
일반적으로 화학결합의 분리가 일어나는 반응
화학반응의 종류
-이성질화 반응
-합성반응
-분해반응
-치환반응
-산・염기 반응
-산화・환원 반응
-연소 반응
1.활성화 에너지
성냥을 태우기 위해 마찰력에 의한 열이 필요
* 활성화에너지: 화학반응을 일으키는데 필요한 최소의 에너지
* 활성화물(Activated Complex, 활성착제) : 반응생성물의 중간적 구조를 갖는 고에너지 전이물질
2.반응 속도
화학반응은 조건에 따라 그 진행속도가 달라진다.
①온도: 일반적으로 반응온도가 10℃ 상승할 경우, 반응속도는 약 2배 증가
→반응물질의 운동에너지 증가
아레니우스 방정식(Arrhenius Equation): 반응속도는 온도와 활성화 에너지의 함수
②농도: 반응물질의 수 증가에 따른 충돌 횟수가 증가 → 반응이 일어날 확률의 증가
화학 반응이 일어나려면 반응하는 물질끼리 충돌이 일어나야함.
* 유효충돌: 충돌을 한다고 해서 다 반응이 일어나는 것이 아니라 반응가능성이 높은 방향으로 충돌하는 것. 유효충돌이 많을수록 반응속도는 빨라진다.
농도의 증가 → 입자수의 증가 → 충돌 횟수의 증가 → 반응 속도의 증가
③촉매: 반응속도를 변화시키고 자신은 변하지 않는 물질.
활성화에너지를 낮추어주어 반응이 쉽게 일어나도록 함
정촉매 : 활성화 에너지 작게 → 반응속도 빨라짐
부촉매 : 활성화 에너지 크게 → 반응속도 느려짐
촉매를 사용해도 반응열은 변하지 않는다.
3. 반응의 방향
화학반응은 에너지가 감소하는 방향으로 진행된다. → 안정한 상태의 물질로 변화한다.
화학반응은 무질서도가 증가하는 방향으로 진행된다. →열역학 제 2법칙
자발적인 반응은 항상 엔트로피를 증가시키는 방향으로 일어난다.
4.반응속도식
화학반응속도(v)는 일반적으로 반응물질의 농도와 관련이 있다.

■화학평형과 평형이동
* 화학평형: 반응이 완결되지 않고 도중에서 정지한 것과 같은 상태.
정반응과 역반응의 속도가 동일한 상태
→가역반응
→조성이 일정
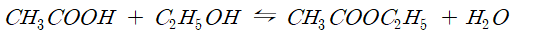
* 평형이동: 화학평형상태의 조건을 바꾸면 정반응 또는 역반응이 촉진되어 조성이 변한 새로운 평형이 이루어진다.
1.평형이동의 법칙
평형이동의 법칙(르 샤틀리에)
화학평형상태에 있는 시스템의 조건을 바꾸면 그 변화의 영향을 될 수 있는 대로 적게 하는 방향으로 평형이 이동한다.
■암모니아의 합성과 평형이동
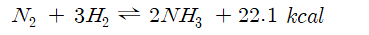
상온・상압의 조건에서 암모니아 생성량은 매우 적다.
암모니아의 생성량을 증가시키는 방법
평형상태의 조건을 바꾸면 그 안에 포함되어 있는 암모니아의 양이 변한다.
NH3의 생성이 많은 쪽으로 평형을 이동
→냉각, 가압, NH3를 바로 제거
1.압력의 변화
기체반응의 경우에 적용
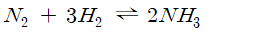
화학반응식의 계수를 고려
.0℃, 1기압에서 반응물 4몰로부터 생성물 2몰 발생
.기체 4몰의 부피는 2몰의 기체의 2배
.압력이 증가하면 반응물이 더 큰 영향을 받는다.
.평형이 정반응쪽으로 이동
2.온도의 변화
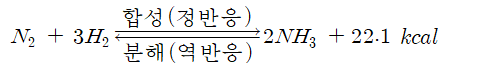
정반응 방향은 발열반응
.암모니아 생성에 따라 열이 발생
.반응온도를 높이면 발열을 줄이는 역반응쪽이 우세
.반응온도에 따른 기체의 운동에너지도 고려
3.농도의 변화
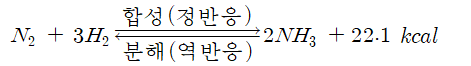
평형상태에서 한 물질의 농도를 증가시키면 그물질의 농도를 감소시키는 방향으로 평형이동
평형상태에서 한 물질의 농도를 감소시키면 그물질의 농도를 증가시키는 방향으로 평형이동
암모니아가 생성되면 바로 배출, 암모니아는 항상 평형 농도보다 낮아 정반응이 우세
4.촉매의 사용
촉매는 활성화에너지를 낮추어 반응속도를 빠르게 한다.
평형에 이르는 속도를 단축시킨다.
암모니아 제조시 다공성 물질을 촉매로 사용
※촉매는 화학평형을 이동시킬 수는 없다.
5.암모니아의 제조
1:3의 몰비로 혼합시킨 질소와 수소를 200~300기압으로 기압하여 500℃ 전후로 가열한 합성탑으로 보내 암모니아 합성.
반응 후 가스 중의 암모니아 농도는 15%내외로 냉각하여 회수, 남은 가스는 순환하여 재사용.
'환경화학' 카테고리의 다른 글
| 화학과, 화학공학, 취업깡패 등 방통대 환경화학 요점 정리 8. 전해질용액과 산・염기 (0) | 2023.01.31 |
|---|---|
| 화학과, 화학공학, 취업깡패 등 방통대 환경화학 요점 정리 7. 기체의 성질 (1) | 2023.01.30 |
| 화학과, 화학공학, 취업깡패 등 방통대 환경화학 요점 정리 5. 용해 (0) | 2023.01.27 |
| 화학과, 화학공학, 취업깡패 등 방통대 환경화학 요점 정리 4. 화학의 기본법칙과 반응식 (1) | 2023.01.26 |
| 화학과, 화학공학, 취업깡패 등 방통대 환경화학 요점 정리 3. 화학량과 화학결합 (0) | 2023.01.26 |



